Partea 2: Simptomele clinice ale tulburărilor microbiome ale pielii. Pentru a citi partea întâi, faceți clic aici.
O considerație majoră în susținerea homeostaziei pielii este echilibrul dintre bariera pielii și microbiomul acesteia. Reacțiile inflamatorii ale pielii și potențialele infecții pot apărea direct ca urmare a unei bariere compromise și a TEWL.
Microbiomul poate deveni dezechilibrat de procese inflamatorii cauzate de impacturi externe sau predispoziții endogene, mecanismele de protecție din epidermă fiind afectate. Proteinele filagrine joacă un rol important în neurodermite și eczeme, deoarece pot afecta dezvoltarea structurii keratinei în timpul procesului de cornificare sau ca o aberație a degradării AMP-urilor care afectează relația simbiotică cu bariera pielii și microbiomul, prin instigarea și dezvoltarea în continuare a agenților patogeni. Inflamația se prezintă frecvent pe măsură ce sistemul imunitar reacționează la o reacție în cascadă alimentată de mediatorii inflamatori.
Atunci când răspunsurile imune sunt poziționate împotriva agenților neinfecțioși, acești mediatori contribuie la patologii ale pielii care implică inflamație nerezolvată sau cronică. Pielea se caracterizează printr-un metabolism activ al lipidelor, iar acizii grași joacă roluri cruciale atât în ceea ce privește integritatea structurală, cât și funcționalitatea, atunci când sunt transformați în mediatori bioactivi.
icosanoidele, endocannabinoidele și sfingolipidele sunt astfel de lipide bioactive cheie, strâns implicate în biologia pielii, inflamație și imunitate.
Afecțiunile țesutului conjunctiv (rozacea) și tipurile de piele hipersensibile cu afectare vasculară pot prezenta frecvent procese inflamatorii atunci când se utilizează creme dense care pot instiga un raport de bacterii anaerobe și aerobe. Prin reducerea oportunității dezechilibrelor microbiene, riscurile pentru dezvoltarea inflamației pot fi descurajate. [10,11,12]
A fost bine demonstrat că sănătatea pielii este poziționată pentru stabilitate prin integritatea și aspectele funcționale ale stratului cornos și imunitatea pielii. Tratamentele vizate care protejează și îmbunătățesc funcția de barieră vor ajuta la susținerea managementului tulburărilor microbiome de pe piele.
Stabilitatea microbiomului, biofilmul și relația cu stratul cornos reprezintă piatra de temelie pentru homeostazia integrală. Cel mai important, aplicațiile estetice, modalitățile și practicile de îngrijire la domiciliu trebuie evaluate cu atenție pentru a evita capcanele care pot instiga inflamația și pot influența o barieră a pielii compromisă.
Acneea vulgară – Factorii primari care contribuie la dezvoltarea acneei includ hipersecreția de sebum, proliferarea anormală, diferențierea keratinocitelor în foliculul de păr, colonizarea bacteriană, dezechilibrele hormonale și enzima alfa 5 reductază care contribuie la dezvoltarea DHT – dihidrotestosteron. Se crede, de asemenea, că bacteria comensală C. acnee mediază răspunsul inflamator și duce la leziuni inflamatorii subclinice de acnee. C. acneea este capabilă să prospere folosind proteaze pentru a elibera aminoacidul arginina din proteinele pielii și lipaze pentru a degrada lipidele trigliceridelor din sebum. Acest lucru eliberează acizi grași liberi, care promovează aderența bacteriană.
Lipaza, proteaza, hialuronatul și liaza, contribuie la degradarea țesuturilor. Lipaza atrage neutrofilele și hidrolizează trigliceridele de sebum în acizi grași liberi, inducând inflamație și hipercheratoză. Factorii dietetici pot influența, de asemenea, dezvoltarea acneei, iar o dietă care include alimente cu un amestec complex de grăsimi, indice glicemic ridicat și lactate poate agrava acneea prin creșterea IGF-1 (factor de creștere-1) și a insulinei. Dieta influențează, de asemenea, microbiota intestinală și dovezile sugerează că o dietă săracă în fibre și bogată în grăsimi provoacă modificări fundamentale în microbiota intestinală, producând boli metabolice și inflamatorii ale pielii [8,12]
Dermatita atopică – Dermatita atopică se caracterizează prin împiedicarea funcției de barieră epidermică și un răspuns imunitar hiperactiv. Modificările din piele și microbiom intestinal au fost legate de un microbiom de piele perturbat și AD. Staphylococcus aureus apare adesea pe pielea uscată și inhibă prezența microorganismelor comensale care pot contribui la sensibilitatea pielii, iritația și o pierdere substanțială a biodiversității în microbiomul pielii.
Nivelurile metabolitului antimicrobian sfingozină și peptidele antimicrobiene catelicidină și defensinele B2 și B3 sunt reduse în pielea subiecților cu AD. Acești factori contribuie la creșterea riscului de infecții cutanate în AD. [13] Pentru a promova în continuare colonizarea, diverse stafilococi pot produce, de asemenea, joncțiuni care promovează atașarea la piele și proteaze care eliberează nutrienți din stratul cornos.
Psoriazisul – Psoriazisul este o boală multifactorială și adesea greșit înțeleasă, care implică o inflamație dereglată și este atât mediată imun, cât și influențată genetic, împreună cu factori de mediu, cum ar fi dieta, stilul de viață și istoricul de sănătate. Psoriazisul este asociat cu inflamația crescută a pielii, hiperproliferarea keratinocitelor și hiperactivarea IL-17, celulelor T și celulelor dendritice inflamatorii. S-a constatat că psoriazisul este exacerbat de Staphylococcus aureus și Streptococcus pyogenes , viruși precum retrovirusurile endogene HPV și ciuperci precum Malassezia și Candida albicans . S-a observat că Corynebacterium , Staphylococcus , Propionibacterium și Streptococcus sunt semnificativ crescute în leziunile psoriazice. Modificările microbiomului intestinal pot activa un statut proinflamator sistemic, care poate contribui la patogenia bolii. Rolul afilierii intestinului-piele în etiopatogenia psoriazisului a fost recunoscut atât în modelele umane, cât și în cele animale de psoriazis. [14]
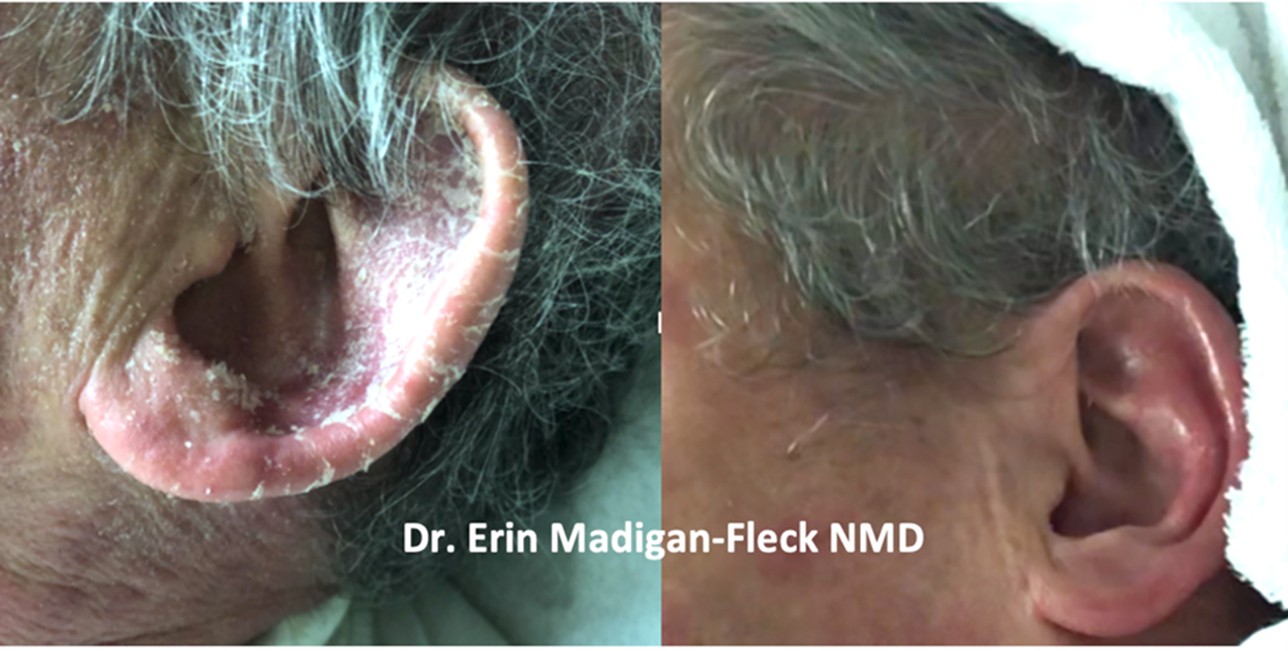
Următoarele imagini arată rezultatele înainte și după pentru un pacient de 64 de ani cu neurodermatită și psoriazis.
Ingredientele țintă ale unguentului pentru repararea barierei au constat din fosfatidilcolină, primulă de seară, uree, ulei de floarea soarelui și ulei de semințe de kiwi.

Rozaceea – Considerațiile clinice primare ale rozaceei includ dereglarea imunității înnăscute și adaptive, semnalizarea neurovasculară, inflamația cronică și creșterea excesivă a organismelor comensale ale pielii. S-a demonstrat că generarea de specii reactive de oxigen este crescută la unii pacienți cu rozacee, ca urmare a unui răspuns imun înnăscut modificat și contribuie la mecanismele inflamatorii ale rozaceei. Demodex folliculorum , Bacillus oleronius , Staphylococcus epidermidis și Cutibacterium acnes au fost, de asemenea, legate de patogeneza rozaceei. Rozaceea poate prezenta, de asemenea, o creștere a densității atât a Demodex brevis, cât și a D. folliculorum și o asociere între D. folliculorum și markerii inflamatori sugerează o activare a sistemului imunitar înnăscut .
Staphylococcus epidermis a fost corelat cu relația dintre sensibilitatea pielii și prezintă un microbiom variabil cu o diversitate bacteriană mai mică și un număr mai mic de S. epidermidis decât pielea nesensibilă. Pielea afectată de rozacee are o expresie mai mare a peptidelor antimicrobiene catelicidine care sunt exprimate atât de leucocite, cât și de celulele epiteliale. Acest lucru poate duce la vasodilatație, angiogeneză și depunere de matrice extracelulară, care în cele din urmă contribuie la dezvoltarea unei stări cutanate disbiotice în rozacee. Activarea citokinelor observată în rozacee (inclusiv interleukina-8 (IL-8) și factorul de necroză tumorală alfa (TNFα)) promovează angiogeneza, evidențiind o cauză potențială a telangiectaziei proeminente de lungă durată, adesea prezentate în rozacee. [15]
Pentru a continua vizionarea articolului trebuie să vă înregistrați. Dacă nu aveți cont, folosiți formularul de mai jos.